
NEWS
新闻中心
SERVERS
服务项目
发布时间:2023-03-17
当前,斑马鱼基因编辑技术在基因敲除、基因敲入、转基因订制及表观遗传修饰等方面的应用日益广泛。环特生物,作为全球斑马鱼技术应用领导者,致力于为客户提供斑马鱼基因敲入、敲除、敲降、定制转基因技术服务及斑马鱼疾病模型开发等专业的基因编辑技术服务,并助力国内外科研工作者们在各类期刊发表了近200篇科研文章。仅2022年,环特生物又助力10余篇高分(最高IF=23.17)科研文章登顶多家顶级期刊,如Nature Communications、Journal of Hematology & Oncology等。
上一期,我们分享了2篇环特斑马鱼技术助力发表的高分科研文章(IF=23.17、17.694,详情点击:IF=23.17!| 看环特斑马鱼技术如何助力10余篇高分科研文章发表,助推各类疾病研究!(一)),本期,我们接着来看2篇由环特生物助力发表的最新科研文章~~~
01、影响因子(IF):11.357
文章题目:《BDE-99 Disrupts the Photoreceptor Patterning of Zebrafish Larvae via Transcription Factor six7》
发表期刊:Environmental Science & Technology
影响因子(IF):11.357
JCR分区:Q1
第一单位:同济大学
DOI: 10.1021/acs.est.1c08914
文章主题:
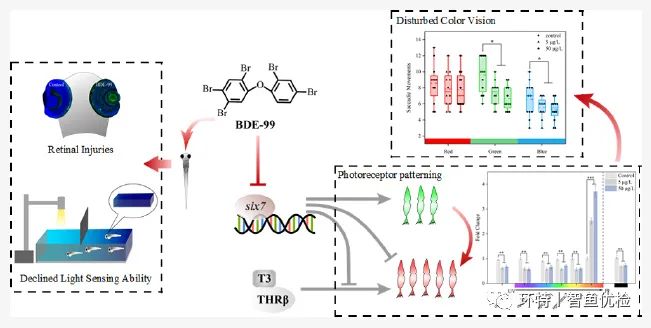
本研究揭示了转录因子six7在一种五溴二苯醚(BDE-99)诱导的斑马鱼视锥细胞图式化发育异常中的重要作用,首次明确了six7在BDE-99发挥视觉毒性中的作用,为理解PBDEs对斑马鱼的视觉损伤机制提供了全新的视角,并揭示了斑马鱼光受体细胞图式化过程中两种调控因子six7和TH信号之间潜在的相互作用。
多溴二苯醚(PBDEs)是曾经使用最广泛的溴代阻燃剂,在水、室内空气和日常食物中均可检测到,其暴露与糖尿病肥胖和神经发育缺陷等代谢性疾病密切相关。BDE-99是商用多溴lianben醚(PBDEs)的主要成分(占42-48%),多溴二苯醚(PBDEs)有可能会损害斑马鱼的视力发育。
该项研究中,研究人员对斑马鱼进行了为期5天的BDE-99暴露(表观浓度分别为5和50 μg/L)。结果表明,50 μg/L 的BDE-99显著抑制了斑马鱼的趋光行为和眼动反应,但并未影响其游动能力,表明BDE-99对于仔鱼的感光功能有显著的损伤效应。通过组织病理学和生物化学手段,发现光感受细胞,特别是视锥细胞,是BDE-99的主要作用靶点。
通过进一步探究BDE-99对仔鱼的视锥细胞发育和色觉感知功能的影响,研究人员发现BDE-99仅诱导长波视蛋白opn1lw1(吸收波长值最大的亚型)的表达而抑制其他视蛋白的表达,且这一规律也体现在斑马鱼的色觉感知功能上。
考虑到甲状腺激素(TH)信号正是opn1lw1表达的必要诱导因子,研究人员开展了甲状腺素T3暴露的阳性对照试验,发现BDE-99对仔鱼视蛋白表达和色觉感知的影响作用和T3的效应高度相似。然而,使用甲状腺素受体拮抗剂的挽救实验并非能完全挽救BDE-99的损伤作用(特别是中波视蛋白),表明还可能存在其他调控因子参与BDE-99诱导的视锥细胞图式化发育异常。
环特贡献:
协助完成six7在视锥细胞图式化发育过程中的调节作用研究,通过在斑马鱼中瞬时敲降和过表达six7基因,揭示了转录因子six7在一种五溴二苯醚(BDE-99)诱导的斑马鱼仔鱼视锥细胞图式化发育异常中的重要作用。
02、影响因子(IF):9.039

文章题目:《Humanized zebrafish as a tractable tool for in vivo evaluation of pro-myelinating drugs》
发表期刊:Cell Chemical Biology
影响因子(IF):9.039
JCR分区:Q1
第一单位:德国波恩大学药物生物学研究所
DOI: 10.1016/j.chembiol.2022.08.007
文章主题:
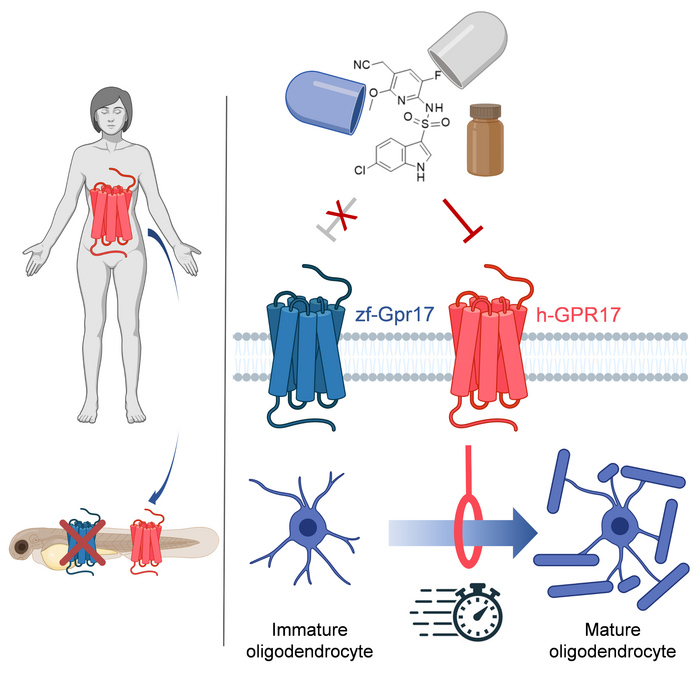
斑马鱼通常用于寻找可能的抗疾病活性物质。德国波恩大学的研究人员通过使用生化和成像技术,可视化了斑马鱼(zf)-gpr17在少突胶质细胞发育的不同阶段的表达,从而证明了斑马鱼类和哺乳动物之间的物种保守表达。
斑马鱼和人类都有GPR17受体,本项研究中,鱼的受体被人类的受体所取代,这使得通过人源化斑马鱼来寻找多发性硬化症药物成为可能。作者通过遗传功能丧失和挽救实验证明了zf-Gpr17的物种保守功能。
最后,借助GPR17人源化斑马鱼,为体内分析通过靶向抑制人GPR17而起作用的化合物提供了原理证明。研究人员在对GPR17受体的初步研究中将部分受体基因替换为人类的对应基因,即负责接收分子信号的结构。实验结果证明,这种新的镶嵌基因在鱼幼体中功能正常。在试管中,一种抑制人类GPR17受体的分子也加快了转基因鱼体内成熟少突胶质细胞的形成。预计GPR17人源化斑马鱼将显著改善对有效促髓鞘形成药物疗法的研究。
环特贡献:
构建斑马鱼GPR17敲除品系。